
MAH(藥品上市許可持有人)申請
1.加快研發機構實現批文產品上市。 2.幫助醫藥公司實現批文產品轉讓。 3.協助藥企實現受托生產。
參考價格 ¥0.00 ¥0.00
典型案例 中國中醫科學院:MAH申請







藥品上市許可持有人(MAH)
藥品上市許可持有人是指取得藥品注冊證書的企業或者藥品研制機構等。申請人為境外企業的,應當指定中國境內的企業法人辦理相關藥品注冊事項。
MAH的義務
1.藥品全生命周期管理責任
2.建立藥品質量保證體系并定期審核
3.建立藥品上市放行規程并嚴格執行
4.建立并實施藥品追溯制度
5.建立年度報告制度 (每年向省級藥監部門報告)
6.中藥飲片生產企業履行藥品上市許可持有人的相關義務
7.境外藥品上市許可持有人的相關義務
8.藥品上市后研究
9.藥物警戒管理
申請成為MAH的權利
1.依法自行生產或委托生產藥品
2.依法自行銷售或委托銷售藥品:藥品上市許可持有人從事藥品零售活動的,應當取得藥品經營許可證
3.依法委托儲存、運輸藥品
4.依法轉讓藥品上市許可(國家藥監部門批準)
5.醫藥代表備案管理
申請藥品上市許可持有人(MAH)常見的問題
· 個人能否成為MAH?研發機構、批發企業想要申請成為MAH該怎么辦?
· 申請MAH需要什么條件?MAH如何解決委托生產、委托銷售的問題?
· 如何建立MAH體系?難度在哪?
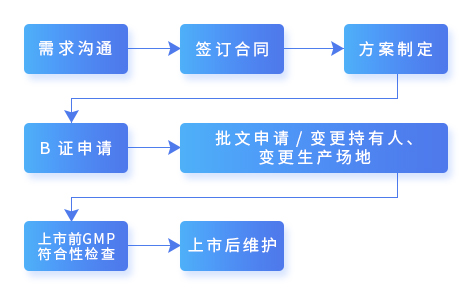
· MAH申請的大致流程是什么?是先變更生產場地還是先變更持有人?
· MAH申請過程中主要涉及到哪些監管部門?

1. MAH體系差距分析與MAH體系建立,包括質量保證體系和藥物警戒體系等
2. 協助企業搭建組織架構,對關鍵人員進行培訓
3. 協助企業滿足設施設備要求
4. 提供醫藥物流相關人員培訓
5. 協助企業申請藥品生產許可證B證
6. 輔導企業獲得批文/變更持有人、變更生產場地
7.輔導通過藥品生產現場檢查、注冊現場檢查、藥品上市前GMP符合性檢查
8.協助企業上市后的長期維護,為企業搭建軟件體系

分享










